1.什么是PD-1/PD-L1?
PD-1(programmed death-1)全称为“程序性死亡受体1”,分布在T淋巴细胞表面,它被激活后,会对淋巴细胞的免疫功能起到抑制作用,属于“免疫检查点”(checkpoint)。
PD-L1(programmed death-ligand 1)全称为“程序性死亡受体-配体1”,分布在癌细胞表面。
当PD-1与PD-L1结合后,PD-1被激活,就会抑制T淋巴细胞的功能,失去增殖和活化的能力,无法有效地清除肿瘤细胞。
2. 什么是PD-1/PD-L1抑制剂?它们为什么能治疗肿瘤?
PD-1/PD-L1抑制剂是抵抗PD-1或PD-L1的药物,它们的作用是抢先占领PD-1或PD-L1,打断肿瘤细胞的作用链条,“唤醒”淋巴细胞,从而识别和攻击肿瘤。
我们如果将免疫系统理解为一辆“跑车”,那么一旦PD-1与PD-L1结合,就相当于踩下了“脚刹”,而PD-1/PD-L1抑制剂通过阻止二者结合,“松开脚刹”,帮助免疫系统“全速前进”,消灭肿瘤。
3. 肿瘤的免疫治疗,就是指PD-1/PD-L1抑制剂吗?
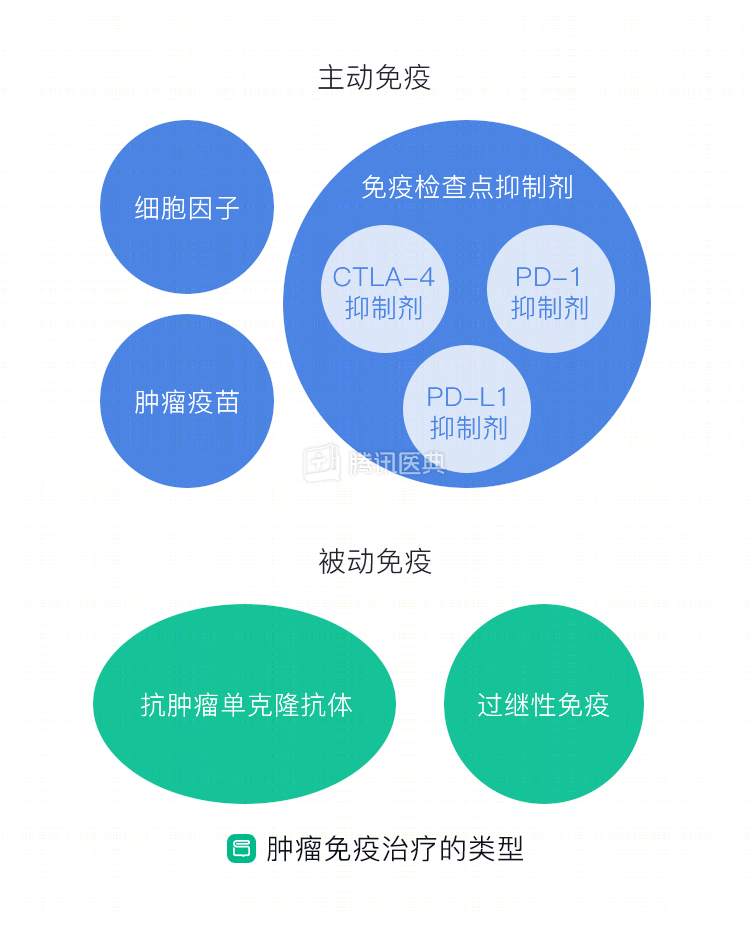
免疫治疗是个非常宽泛的概念。总体上,肺癌的免疫治疗可以分为主动免疫治疗和被动免疫治疗。主动免疫治疗,是指直接作用于患者的免疫系统,诱导它发起对抗肿瘤的免疫反应,这相当于“授人以渔”。它的特点是抗肿瘤作用比较持久,可以产生“免疫记忆”,也就是说,当机体再次遇到相同的抗原,会“识别出来”,产生更强烈的免疫反应。PD-1/PD-L1抑制剂、CTLA-4(细胞毒T淋巴细胞抗原4)抑制剂以及肺癌疫苗都属于这一类。
除此之外,还有被动免疫,被动免疫治疗不需要“动员”患者自身的免疫系统,医生直接将具有抗肿瘤活性的药物或免疫细胞输入患者体内,杀灭肿瘤。这种“授人以鱼”的方法,相比“授人以渔”的主动免疫治疗,疗效持续时间更短。CAR-T(Chimeric Antigen Receptor T-Cell Immunotherapy,即嵌合抗原受体T细胞疗法)就属于被动免疫。
现有的主动免疫和被动免疫治疗详见下图。
4. PD-1/PD-L1抑制剂和“魏则西免疫治疗”是一回事吗?
年轻的滑膜肉瘤患者魏则西接受的免疫治疗,专业上称为DC-CIK免疫治疗。DC(dendritic cells)是“树突细胞”的简称,它是我们体内免疫系统的一种成分——抗原递呈细胞,它能处理肿瘤细胞表面的抗原,并呈递给具有杀伤作用的免疫细胞,比如CIK(Cytokine-Induced Killer,细胞因子诱导的杀伤细胞),两者合作,就可以高效发现和杀灭肿瘤细胞[1]。
从具体操作看,DC-CIK治疗是将患者本人的DC和淋巴细胞提取出来,在体外重新诱导激活并扩增后,再一起输回患者体内。从作用机制上属于被动免疫。而PD-1/PD-L1抑制剂则不同,它们能够阻止T淋巴细胞表面的PD-1与肿瘤细胞表面的PD-L1结合,恢复患者自身T细胞增殖和攻击癌细胞的能力,属于主动免疫。
DC-CIK治疗中,除了Provenge(又叫sipuleucel-T,是一种自体细胞免疫疗法,用于治疗无症状、或症状最轻微的转移性激素难治性前列腺癌)这一技术外,没有获得美国FDA批准用于临床治疗任何肿瘤[2]。而PD-1/PD-L1抑制剂方面,目前已有5个药物获得FDA批准,用于不同类型的肿瘤治疗,分别为Nivolumab、Pembrolizumab、Atezolizumab、Durvalumab和Avelumab。除Avelumab外,其他四个药物都可以用于一部分肺癌患者[3][4][5][6][7]。
5. 它们是像化疗药作用于全身?还是像靶向药直击肿瘤?
PD-1是存在于T淋巴细胞表面的一种蛋白成分(受体),它被激活后,对淋巴细胞的免疫功能起到抑制作用。而肿瘤细胞表面的PD-L1就可以激活PD-1。
无论是PD-1抑制剂,还是PD-L1抑制剂,都能阻断两者的“亲密接触”,从而避免PD-1被激活,解除了对淋巴细胞的抑制,使它能够集中火力攻击肿瘤。在斗争过程中,如果误伤正常细胞,就会造成治疗的不良反应。
传统化疗大多通过静脉给药,作用于全身,它就像“大规模杀伤性武器”,选择性比较差,在杀灭肿瘤的同时,也会对正常组织和细胞造成伤害。靶向治疗是针对特定致癌基因突变的治疗,它就像“激光制导炮弹”,命中率高,威力强,打击目标外的损伤非常小(不良反应小)。但靶向治疗必须要有靶点——特定的基因突变,如果没有突变、或突变发生了变化,就不起作用了。
对比后可发现,PD-1/PD-L1抑制剂的作用方式与化疗和靶向治疗都不太一样,因为后两者是作为武器直接去攻击肿瘤,而PD-1/PD-L1抑制剂本身并不攻击肿瘤,而是通过恢复机体对肿瘤的免疫反应来发挥作用。
6. 为什么大家如此关注这类药物?它有什么优势?
近年来,PD-1/PD-L1抑制剂在多项研究中,疗效数据超过了现行的标准治疗,这些研究的主要结果和临床影响如下表所示。
药物 | 研究 | 主要结果 | 临床影响 |
Nivolumab | Checkmate017 Checkmate057 Checkmate078 | 2015年获得美国FDA批准作为含铂化疗失败后转移性NSCLC患者,或EGFR、ALK突变晚期NSCLC患者的二线治疗 2018 年 9 月,美国 FDA 批准纳武单抗用于治疗转移性小细胞肺癌(small cell lung cancer,SCLC)患者,这些患者对铂基化疗和至少另一种治疗方法无效。 | |
Pembrolizumab | Keynote010 Keynote024 Keynote021 | 在Keynote010研究中,对于PD-L1阳性患者,Pembrolizumab二线治疗完胜多西他赛化疗; 在Keynote024研究中,对于PD-L1≥50%的患者,Pembrolizumab一线治疗完胜铂类为基础的化疗 在Keynote021研究中,Pembrolizumab连用PC化疗方案,相对于单纯PC化疗方案,总体缓解率和无进展生存率有着明显改善 | 2015年获批作为PD-L1阳性的转移性NSCLC二线治疗。 2016年获批用于PD-L1≥50%、无EGFR或ALK突变晚期NSCLC的一线治疗 2017年FDA批准pembrolizumab与培美曲塞和卡铂联合用于治疗既往未治疗的转移性非鳞状非小细胞肺癌(NSCLC)的患者 |
Atezolizumab | POPLAR和OAK | 尽管总生存数据还不成熟,但在二线治疗中,Atezolizumab的ORR和PFS显著优于化疗 | 2016年FDA批准atezolizumab用于治疗含铂治疗期间或进展后的转移性非小细胞肺癌(NSCLC)患者。以及作为EGFR或ALK突变晚期NSCLC患者的二线治疗 |
Durvalumab | PACIFIC | 对同期放化疗后病情没有进展的Ⅲ期NSCLC患者,用Durvalumab作为巩固治疗能显著改善ORR和PFS | 2018年获批用于同期放化疗后疾病没有进展、并且不能手术切除的Ⅲ期NSCLC的巩固治疗 |
面对如此漂亮的成绩单,很难不对PD-1/PD-L1抑制剂倾心。总结这些研究结果可以发现,PD-1/PD-L1抑制剂的优势主要体现在,对于特定人群,疗效优于化疗。而且,由于作用过程中能影响免疫记忆,一旦起效,疗效持久。此外,PD-1/PD-L1抑制剂的不良反应也比化疗少。
相关阅读:
共同审核:广东省人民医院 广东省肺癌研究所 王震副主任医师 黎琳琳医生
参考文献 共 7 篇
[1] Märten A, et al..Interactions between dendritic cells and cytokine-induced killer cells lead to an activation of both populations.[J].J Immunother. 2001;24(6):502–10.